- Et pour aller plus loin
- Voies de recherche
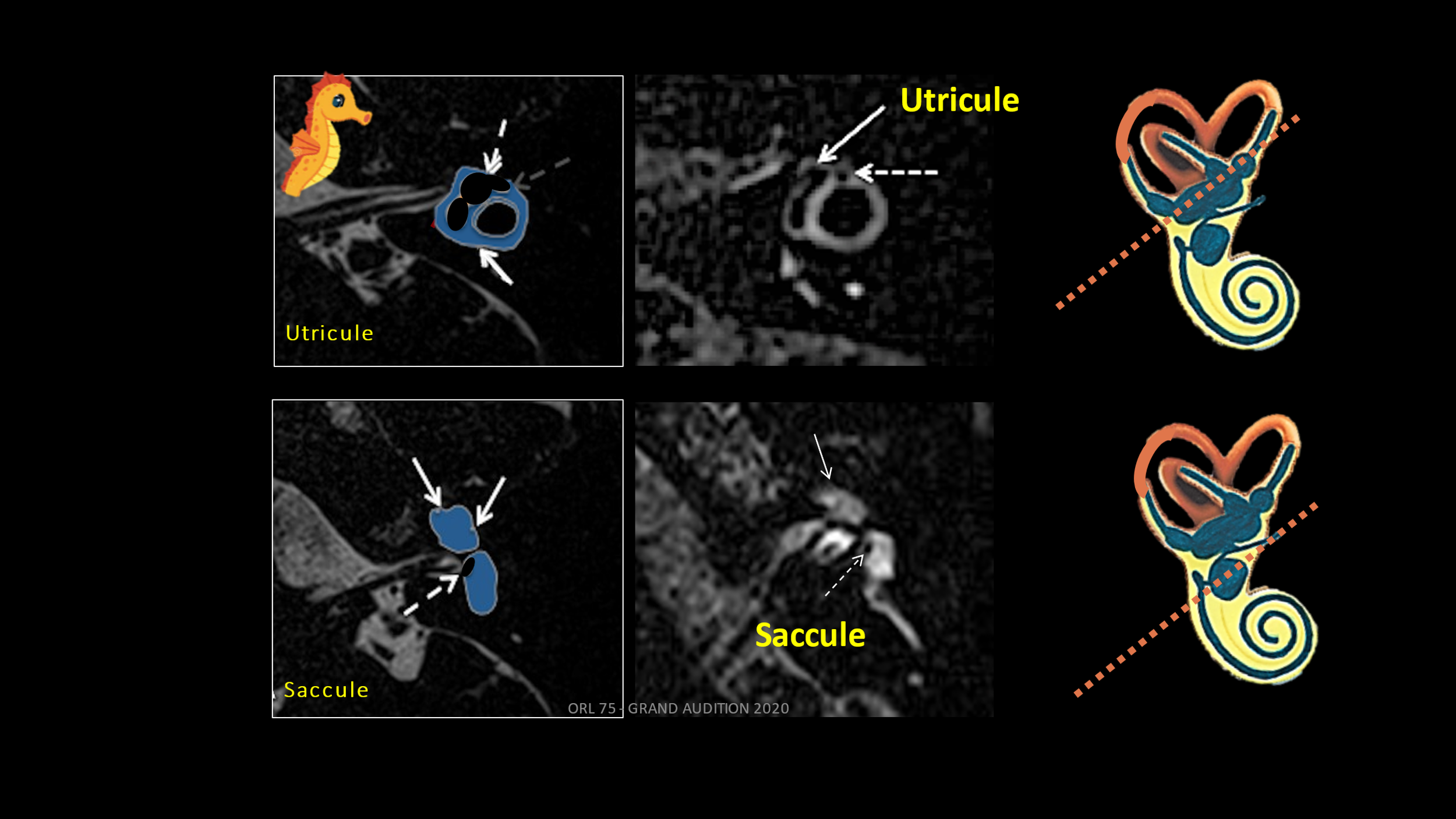
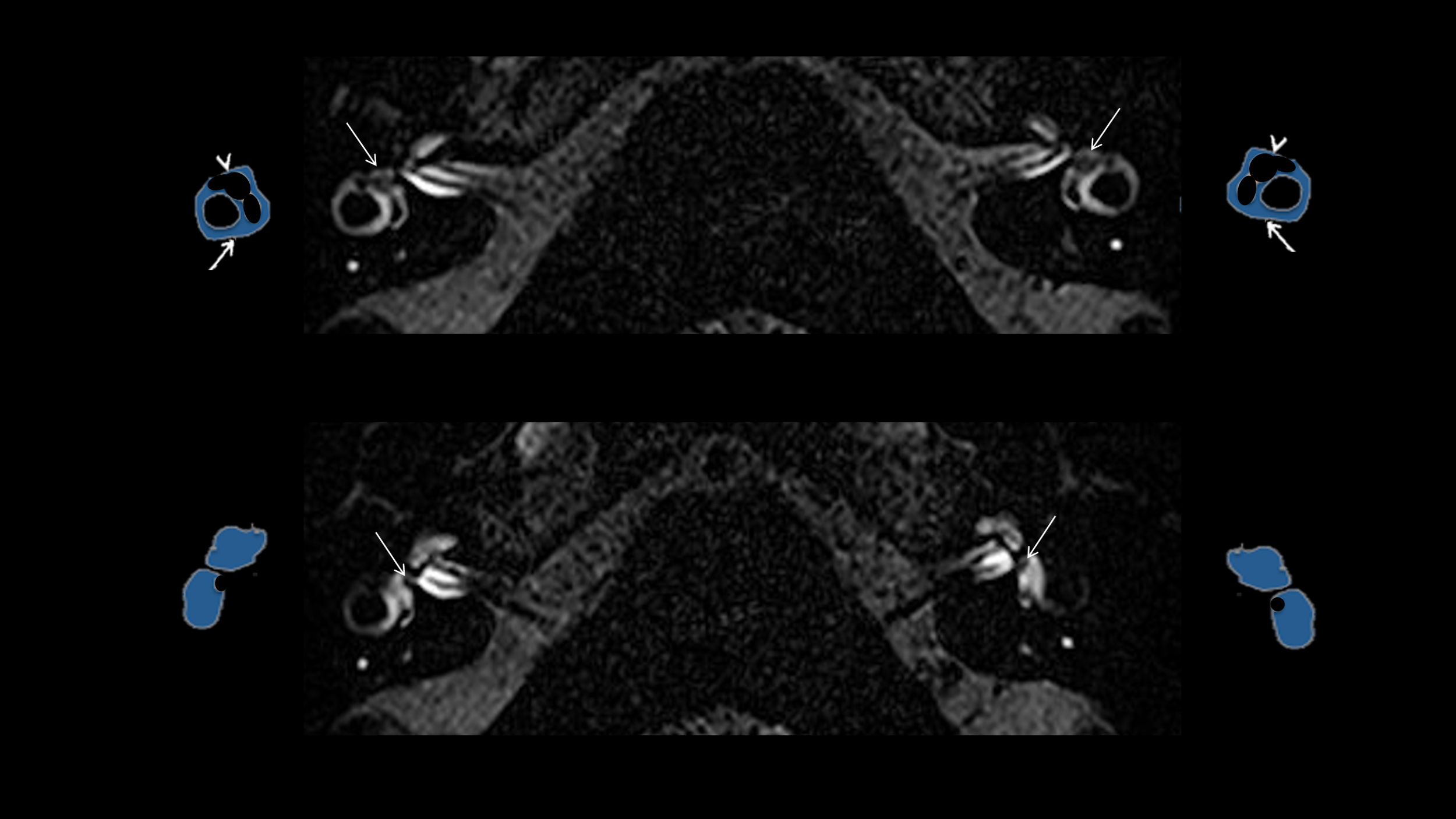
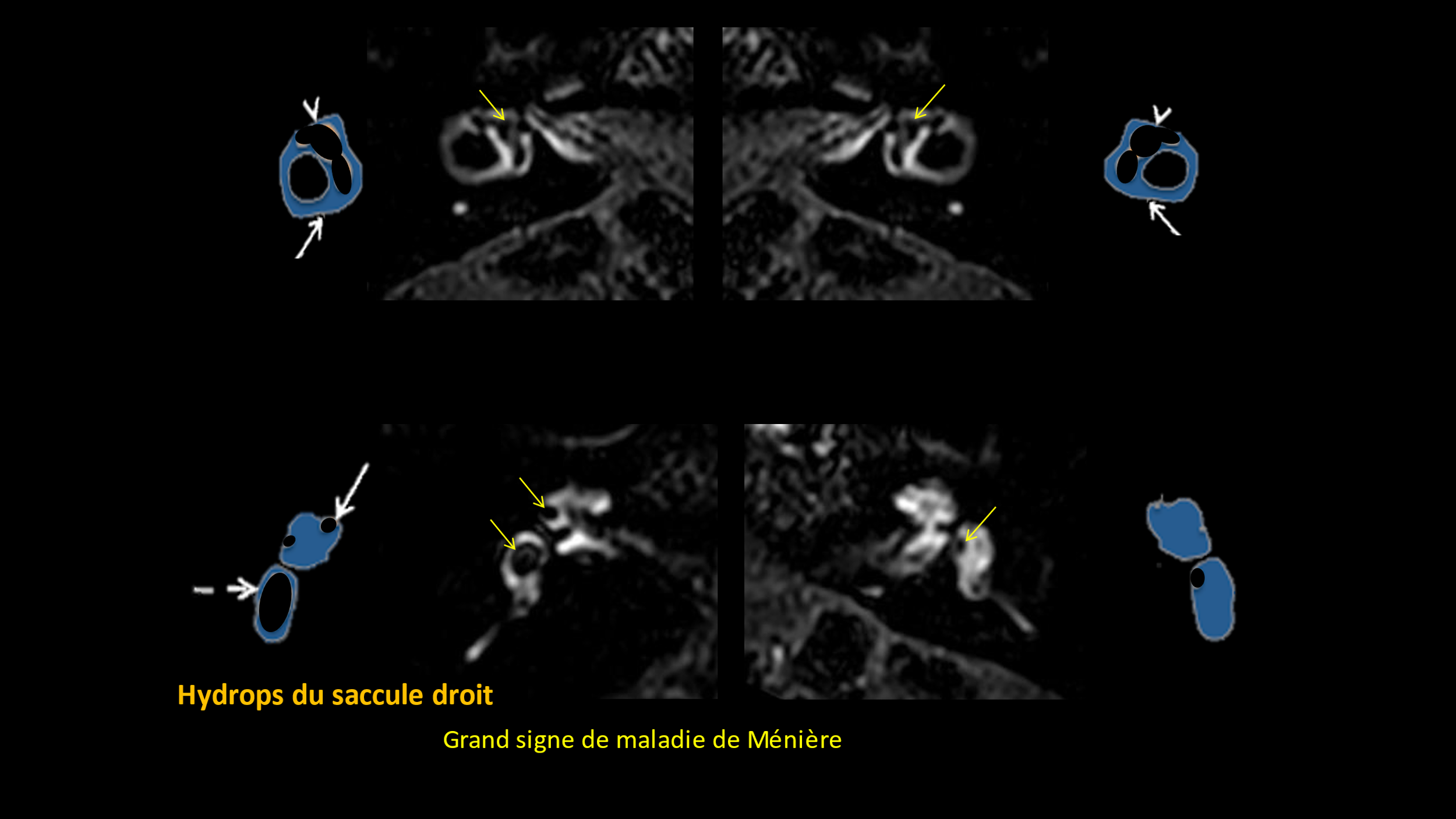
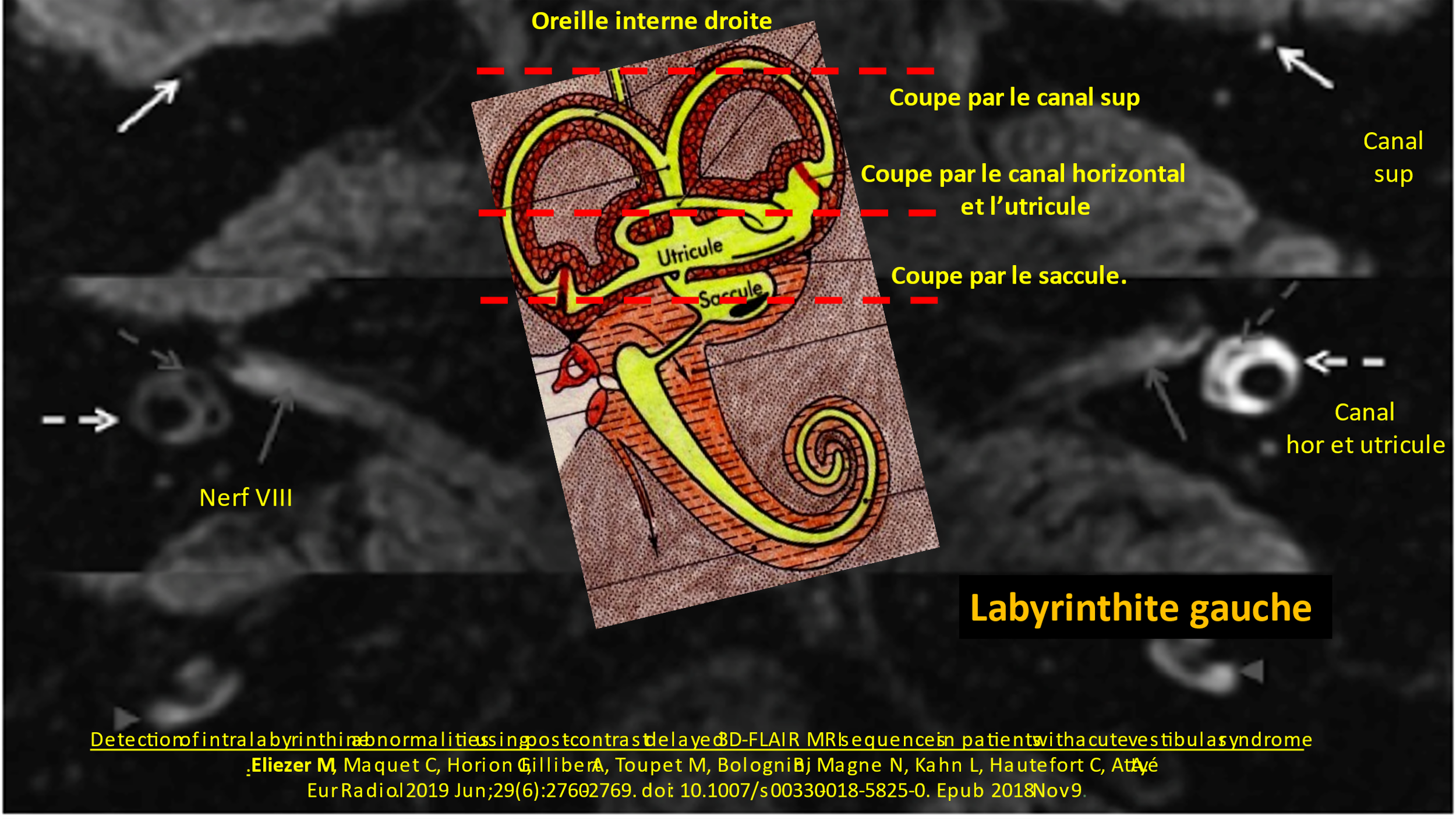
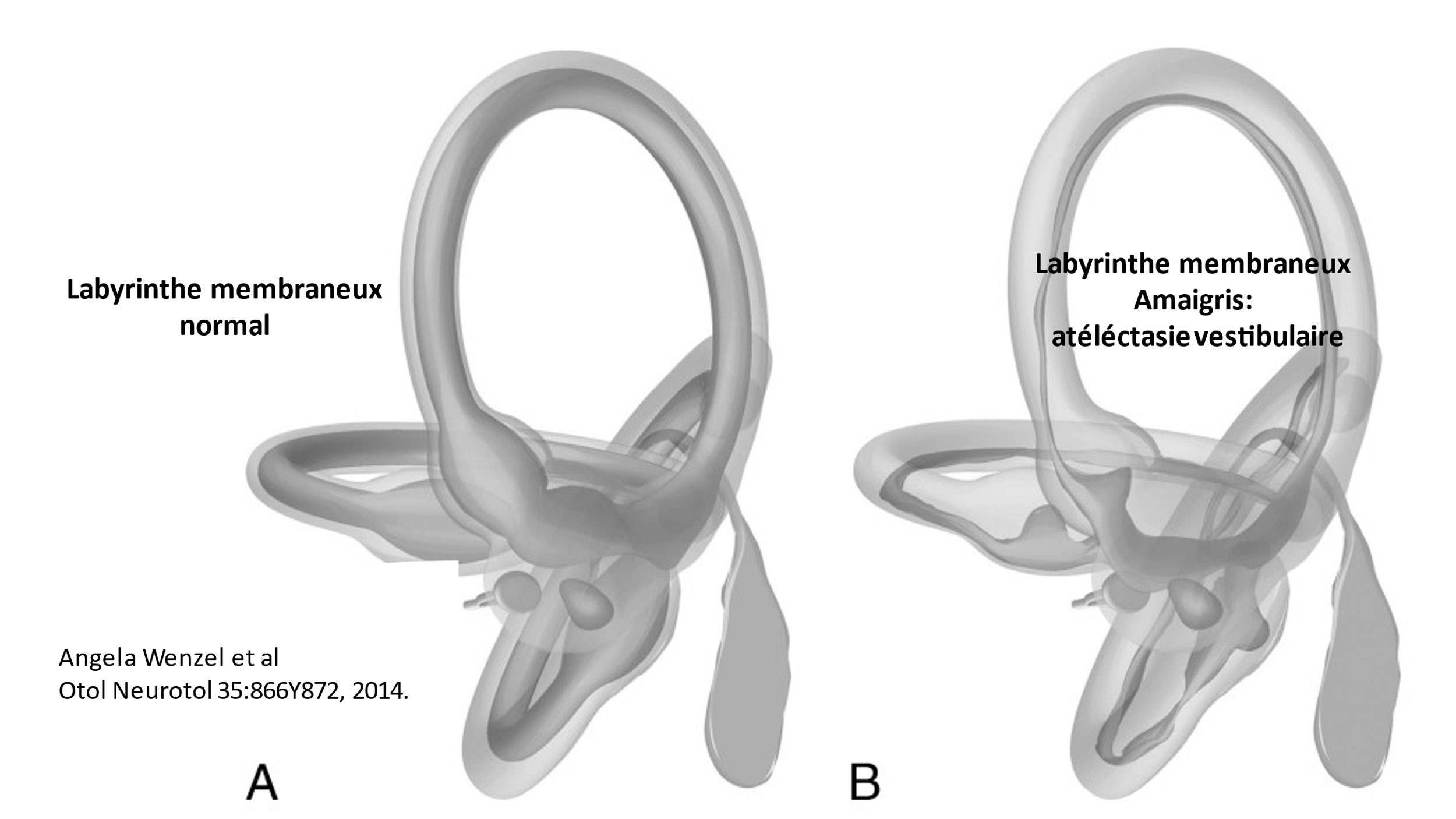
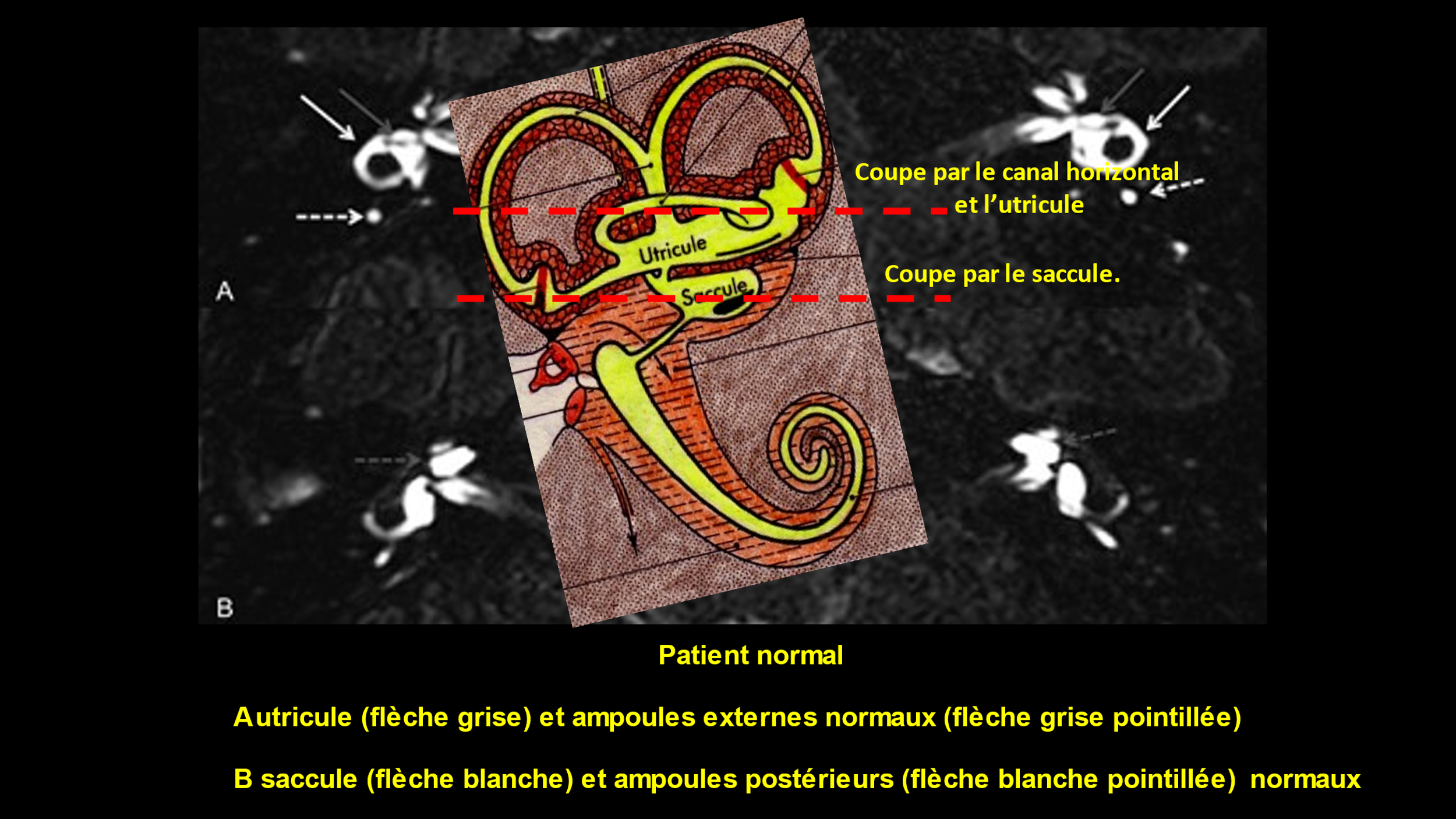
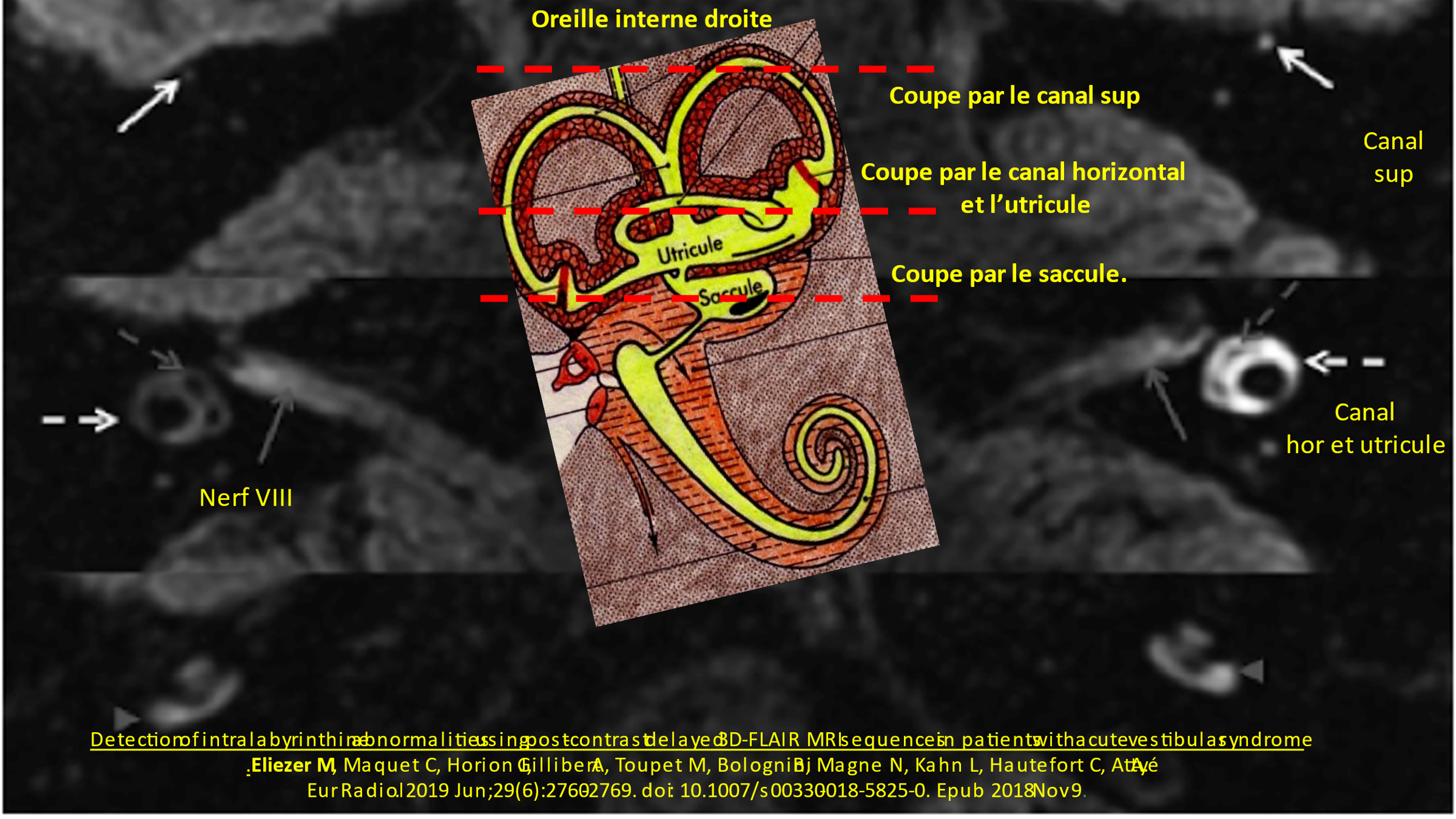
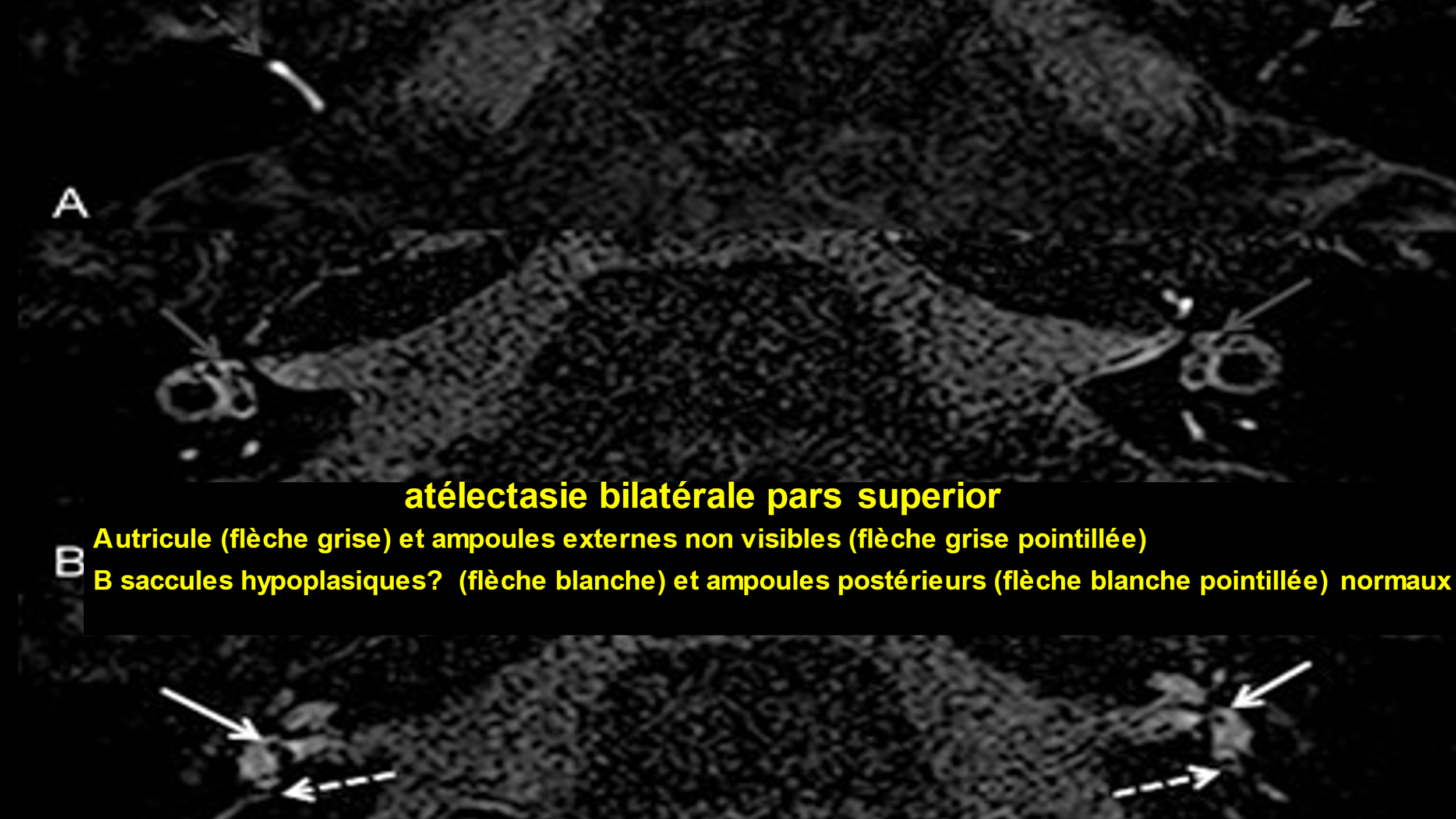
Les techniques récentes d’imagerie, les séquences 3D-FLAIR retardées de l’Imagerie par Résonance Magnétique (IRM), ont donné de nouvelles indications sur diverses maladies de l'oreille interne. L'acronyme FLAIR provient de l'anglais « Fluid Attenuated Inversion Recovery ». L’objectif de la séquence FLAIR est de supprimer le signal des liquides. Cette technique est pratiquée depuis plusieurs années pour des patients atteints de la maladie de Menière. Les médecins se sont aperçus que d’autres anomalies pouvaient être détectées (inflammations, malformations etc.).
Un protocole d’imagerie vestibulaire de pointe a été développé par l’équipe de neuroradiologie du Centre Hospitalier Universitaire de Grenoble et de l’Hôpital Lariboisière à Paris. Son objectif est d'évaluer à la fois la morphologie de l'espace endolymphatique et la perméabilité de la barrière hémato-labyrinthique chez les patients atteints de vestibulopathie bilatérale idiopathique.
Il a fait l’objet d’une étude portant sur 42 patients atteints de VBI qui a montré que ces patients présentaient des anomalies morphologiques de l'espace endolymphatique (Bilateral vestibular atelectasis (VA) a été trouvé chez 21 patients (50%), ou une détérioration de la barrière hémato-labyrinthique dans 59,6 % des cas (1).
Cette étude et les séquences 3D-Flair d’imagerie permettent d’émettre l’hypothèse d’une étiologie ischémique (par réduction de l’apport sanguin aux vestibules) de l’aréflexie vestibulaire, et donc qu’une pathologie microvasculaire serait envisageable.
Chez les patients présentant un déficit vestibulaire bilatéral : l’I.R.M. 3Teslas protocole Hydrops montre, le plus souvent, un effondrement des territoires endolymphatiques : une atélectasie vestibulaire bilatérale et le plus souvent de la partie supérieure du labyrinthe : canal supérieur, canal horizontal, utricule.
Ludovic DROUET
Dans la recherche de facteurs de risque d’atteintes microvasculaires qui puissent participer à la genèse d'une VBI, il y a trois paramètres qui sont très fréquemment rencontrés au niveau sanguin chez les patients atteints de VBI : une augmentation du taux plasmatique de sérotonine, une augmentation de l'homocystéine, et la présence d’anti-cardiolipines (autoanticorps anti-phospholipides), ce qui suggère un facteur d’auto-immunité, voire de thrombophilie.
L’origine microvasculaire serait l’effet synergique de ces trois facteurs de risque.
Mais ces trois anomalies n’étant pas identiques chez tous les patients, un bilan sanguin spécifique est nécessaire ; les résultats devraient permettre d’établir un traitement adapté pour prévenir de complications. Les atteintes déjà constatées sont malheureusement pour l’instant irréversibles.
- La sérotonine plasmatique
La sérotonine est un neuromédiateur qui peut être impliqué dans différents troubles :
- migraines, spasmes artériels, pathologies sur les valves cardiaques
- dépressions, régulation de l’appétit, autisme
- syndrome de l’intestin irritable
- mictions impérieuses
- mal des transports
- troubles du sommeil
- et pathologies microvasculaires (rétiniennes ou cochléo-vestibulaires)…
La sérotonine plasmatique en excès est responsable d'une réaction de spasme au niveau des micro-vaisseaux, en particulier du système vasculaire cochléo-vestibulaire et peut ainsi participer à l'ischémie qui provoque la VBI. Ce spasme est d'autant plus important que la paroi vasculaire est atteinte.
Cette dernière pouvant être altérée par l'homocystéine et l'auto-immunité.
A l’état normal, la sérotonine est produite par des cellules qui sont sur le tube digestif puis captée par les plaquettes sanguines. L'augmentation de la sérotonine plasmatique signifie soit que la sérotonine est libérée trop facilement par les plaquettes soit qu’elle n’est pas captée par les plaquettes.
C'est pourquoi le traitement utilisé en premier essai chez les patients atteints de VBI et présentant une augmentation de la sérotonine plasmatique est un antiagrégant plaquettaire ; l'aspirine (75 ou 100mg).
Le but de ce traitement est d'empêcher l'activation des plaquettes et la libération de sérotonine par les plaquettes. Un deuxième effet est également attendu : empêcher la formation de microthrombi plaquettaires dans la microcirculation.
L'aspirine à faible dose est utilisée à très long cours en prévention cardiovasculaire sans poser de problème (à part un risque hémorragique en cas de saignement). Elle pourrait diminuer le risque de cancer du côlon.
L’aspirine ne peut pas être utilisée chez les patients atteints de VBI et de la maladie de Willebrand, pathologie hémorragique très fréquente. C’est une anomalie de la coagulation due à un déficit partiel en facteur Willebrand (qui sert dans l'interaction des plaquettes au cours des processus d'hémostase et de coagulation). Chez ces patients, on évalue un traitement par inhibiteur de recapture de sérotonine (comme certains antidépresseurs) pour diminuer la sérotonine sanguine totale.
- L’homocystéine sanguine
L'homocystéine est un acide aminé extrêmement réactif et toxique pour les parois vasculaires. L’augmentation du taux d’homocystéine dans le sang, ou hyperhomocystéinémie, entraîne une pathologie vasculaire et peut jouer un rôle dans les atteintes oculaires ou cochléo-vestibulaires. Elle est le plus souvent due à une anomalie sur l’enzyme MTHFR (Méthylènetétrahydrofolate) mais d’autres enzymes peuvent être atteints.
L’existence d’une hyperhomocystéinémie induit la mise en place d’une supplémentation régulière et définitive en vitamines B, dont la vitamine B9. Cette dernière se trouve dans les légumes verts mais la quantité nécessaire ne peut pas être apportée par la simple alimentation car il ne s’agit pas de compenser une carence.
La vitamine B9 est le cofacteur des enzymes du métabolisme de l'homocystéine. La supplémentation augmente le taux de vitamine B9, ce qui booste ces enzymes et fait tomber le taux d'homocystéine : c’est le résultat recherché.
On utilise une dose de vitamine B9 de 5 mg/jour, sous la forme d’acide folique ou d'acide folinique (forme déjà métabolisée de la vitamine B9).
- Les anti-cardiolipines
Ce sont des anticorps que le corps fabrique lorsqu’il est attaqué par un virus, une bactérie, un champignon... Ils vont reconnaître un antigène ou plus précisément son épitope, c’est à dire la partie de l'antigène contre laquelle va être fabriqué l'anticorps.
Les anti-cardiolipines s’opposent aux phospholipides qui constituent les membranes des cellules et à la bêta2-glycoprotéine 1 (protéine β2-GP1) qui se fixe dessus. Cela entraîne un défaut au niveau des cellules endothéliales. On pense que les anti-cardiolipines blessent les cellules endothéliales qui bordent la paroi vasculaire et cet effet est potentialisé probablement à la fois par l’homocystéine et la sérotonine. Cela explique pourquoi c’est l’association des trois qui aboutit aux lésions micro-vasculaires.
- Dosages sanguins
Les patients atteints de VBI sont donc amenés à subir des prises de sang pour que soit établi ce bilan sanguin particulier dont le Centre de référence est le laboratoire de l’hôpital Lariboisière à Paris. C’est le seul laboratoire en France qui dose sur place la sérotonine, immédiatement après la prise de sang, évitant ainsi les délais de transport qui faussent les résultats. C’est aussi là que sont utilisées les techniques de références pour le dosage de l’homocystéinémie et des anti-cardiolipines.
Les tests sanguins doivent être répétés pour vérifier la fiabilité des résultats et les effets des traitements.
Ces examens s’accompagnent maintenant d’une analyse sanguine dont les résultats pourraient permettre d’élaborer une typologie de malades et d’avancer ainsi dans la recherche étiologique.
(1) Electrophysiological and inner ear MRI findings in patients with bilateral vestibulopathy
M.Eliezer, C. Hautefort, C. Van Nechel, U. Duquesne, JP. Guichard, P. Herman, R. Kania, E. Houdart, A. Attye, M. Toupet
Received: 27 November 2019 / Accepted: 24 January 2020
© Springer-Verlag GmbH Germany, part of Springer Nature 2020
- Vestibule, sommeil et rythmes biologiques
Tristan Martin, Gaëlle Quarck, Hervé Normand, Pierre Denise
Le rôle du système vestibulaire dans l’équilibration, la posture et la cognition spatiale est de mieux en mieux connu. Le système vestibulaire est classiquement reconnu comme le principal organe du « sens du mouvement ». Cependant, s’impose progressivement l’idée que le système vestibulaire a une influence beaucoup plus diffuse sur l’ensemble du cerveau, et même sur l’ensemble de l’organisme par l’intermédiaire du contrôle du système nerveux végétatif. Plusieurs équipes, dont le laboratoire COMETE (Caen), ont ainsi montré les relations entre le système vestibulaire et les régulations cardiovasculaires, respiratoires, musculaires, osseuses et endocriniennes. Ces nouvelles connaissances ouvrent des perspectives pour une meilleure compréhension des conséquences et du traitement des dysfonctionnements du système vestibulaire.
Dans ce chapitre, nous décrirons comment un dysfonctionnement vestibulaire peut perturber le sommeil et les rythmes biologiques.
- Sommeil et chronobiologie
La régulation du sommeil est un phénomène complexe encore imparfaitement connu. Un des aspects les plus importants de cette régulation est son organisation temporelle : comment et pourquoi le sommeil survient à certains moments et pour une certaine durée.
Cette alternance entre les états de veille et de sommeil dépend principalement de notre « horloge biologique » centrale. Celle-ci est constituée de plusieurs dizaines de milliers de neurones situés dans une petite zone localisée au-dessus du croisement des nerfs optiques appelée « les noyaux suprachiasmatiques »1. Cette horloge biologique envoie un message rythmique aux centres de régulation de l’organisme, induisant une oscillation entre des périodes d’activité importante et d’activité plus faible des fonctions physiologiques, neuronales et endocriniennes. Les exemples d’oscillations les plus remarquables que l’on peut observer sont les variations de la température, de la mélatonine (hormone associée à la nuit, favorisant l’endormissement chez l’homme) ou le cortisol. L’ensemble de ces « rythmes biologiques », dont l’étude est l’objet de la chronobiologie, permet un fonctionnement harmonieux du corps humain au cours des 24 heures, afin qu’il puisse accomplir au bon moment les activités liées au jour et à la nuit. Le rythme veille-sommeil est également sous la dépendance de cette horloge interne. Les rythmes biologiques sont définis, pour chaque marqueur considéré, par l’heure à laquelle s’observe le niveau maximal (acrophase), le niveau minimal (bathyphase), l’amplitude (différence entre le maximum et le minimum du paramètre), le niveau moyen (Mesor) et surtout la période (une période d’environ 24 heures est appelée « circadienne »).
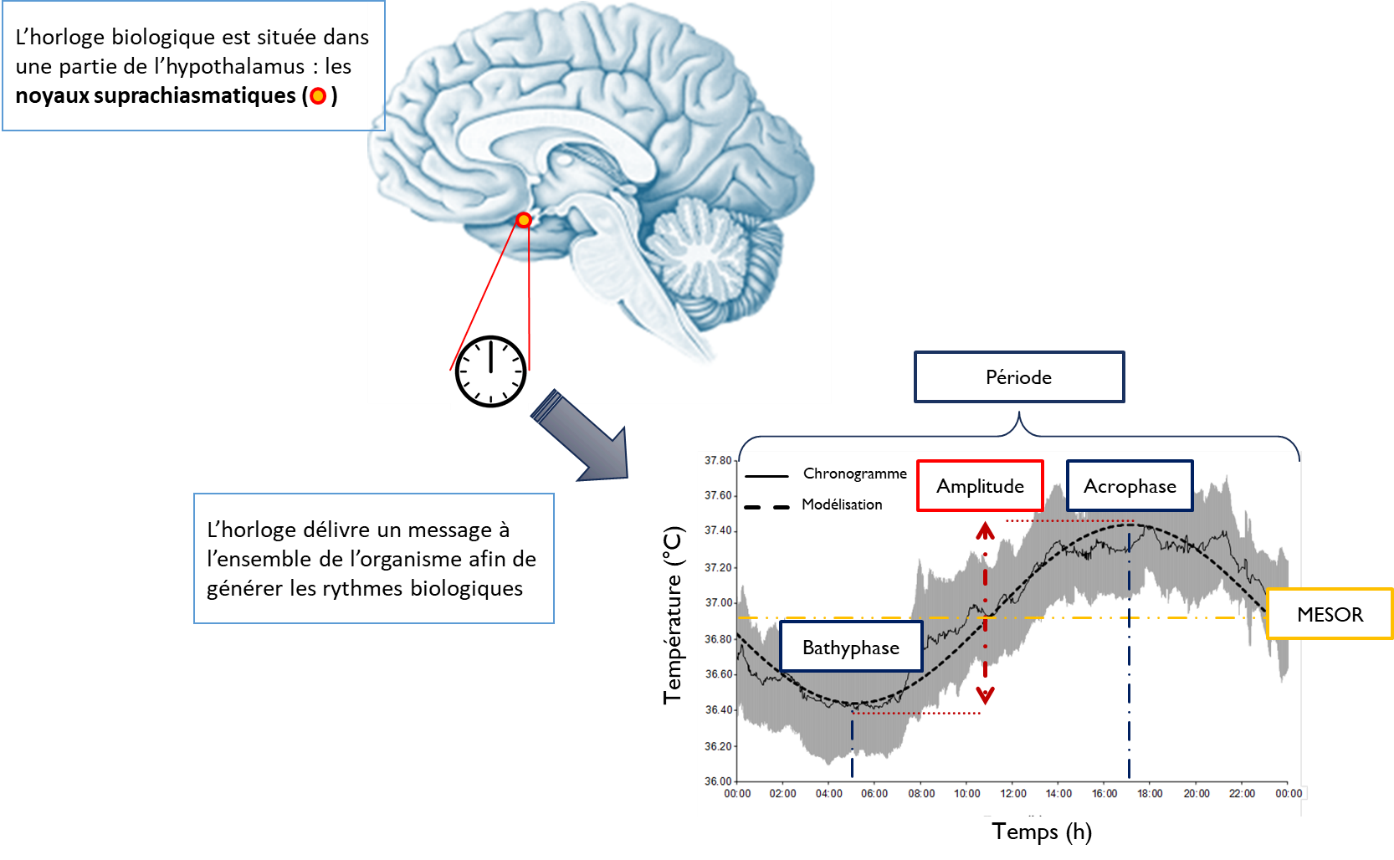 Figure 1 : Illustration de l’horloge biologique et des caractéristiques d’un rythme circadien (celui de la température dans cet exemple).
Figure 1 : Illustration de l’horloge biologique et des caractéristiques d’un rythme circadien (celui de la température dans cet exemple).
La période spontanée de l’horloge interne est légèrement supérieure à 24 heures. Ainsi spontanément et en l’absence de tout repère temporel, comme l’a montré l’expérience d’isolement de 2 mois sous terre de Michel Ciffre dans les années 60, l’être humain décale son sommeil peu à peu et se couche et lève de plus en plus tard. Afin d’agir efficacement en restant en phase avec son environnement, l’organisme doit en permanence resynchroniser son horloge biologique ; pour ce faire, il utilise certains signaux de l’environnement, les « synchroniseurs ». La lumière du jour constitue le principal synchroniseur externe de notre horloge biologique3 et explique les troubles du sommeil observés chez les aveugles et dans les pays nordiques, présentant de longue période d’obscurité. D’autres synchroniseurs dits « non lumineux » ont été découverts, telle que l’activité physique. Pratiquée régulièrement, elle peut resynchroniser le système circadien chez des personnes désynchronisées (travailleurs de nuit, personnes âgées, personnes aveugles…).
- Troubles du sommeil d’origine chronobiologique
Les troubles du sommeil touchent 39% des Français4. Si l’insomnie est la plainte la plus fréquente (21%), elle est souvent intriquée avec les troubles du rythme circadien veille-sommeil. Les troubles des rythmes circadiens (18% des troubles recensés) sont à l’origine de nombreuses perturbations : troubles du sommeil, diminution de la vigilance, déficits cognitif (trouble) et psychomoteurs, perturbations endocriniennes et métaboliques, altérations du système immunitaire. Ils sont également impliqués dans les processus de dérégulations du cycle cellulaire et associés à des pathologies comme le cancer. On observe ces troubles de la rythmicité chez des publics tels que les travailleurs postés, comme comorbidités associées à des pathologies chroniques et dans les situations de décalage horaire après un vol transméridien.
- Vestibule et chronobiologie
Une hypothèse ayant émergé au sein de notre laboratoire COMETE est que le système vestibulaire pourrait transmettre des informations à cette horloge biologique et donc agir comme un synchroniseur. Longtemps restreint à un simple capteur de mouvement de la tête assurant notre équilibre et maintenant la fixation oculaire par l’intermédiaire de réseaux neuronaux localisés au niveau du tronc cérébral (spinal, oculomoteur, cervelet), il s’avère que la sensorialité vestibulaire, en particulier le codage des informations gravitaires et des déplacements linéaires, est bien plus que cela. Ainsi, les informations vestibulaires d’ordre gravitaire semblent moduler de façon majeure le carrefour neuroendocrinien, à savoir l’hypothalamus, et en particulier nos rythmes circadiens. L’existence de connexions anatomiques entre les noyaux vestibulaires et les noyaux suprachiasmatiques (siège, nous l’avons vu de l’horloge biologique centrale) a été démontrée chez le rongeur5.
L’hypothèse que les informations vestibulaires transmises aux centres supérieurs influencent le fonctionnement de l’horloge biologique lorsque l’organisme est en mouvement, a été démontrée chez l’animal. Des animaux placés dans un environnement artificiel les exposant de manière prolongée à une hypergravité (2G), voient leur rythmicité biologique disparaitre pendant la première semaine alors que des souris génétiquement privées de récepteurs gravitaires vestibulaires (organes otolithiques) ne sont pas affectées par cette stimulation6.
A partir de ces travaux, nous avons approfondi les liens fonctionnels entre fonction vestibulaire et rythmicité biologique de manière complémentaire chez l’Homme et l’animal. Nous avons démontré qu’une privation des informations vestibulaires suite à une lésion chimique bilatérale des cellules ciliées vestibulaires induisait des perturbations de la rythmicité biologique chez le rat la semaine suivant la lésion, suivie d’une récupération progressive, probablement grâce à l’influence majeure du cycle jour/nuit7. Chez l’homme, les personnes atteintes d’une aréflexie vestibulaire bilatérale présentent une détérioration du sommeil, marquée par une fragmentation et un niveau d’activité plus élevé durant la nuit. De plus, chez ces patients, par rapport à des participants témoins dont le rythme de la température était corrélé au rythme activité repos, une désynchronisation entre le cycle veille-sommeil et la température corporelle des patients a été observée8 (figure 2).
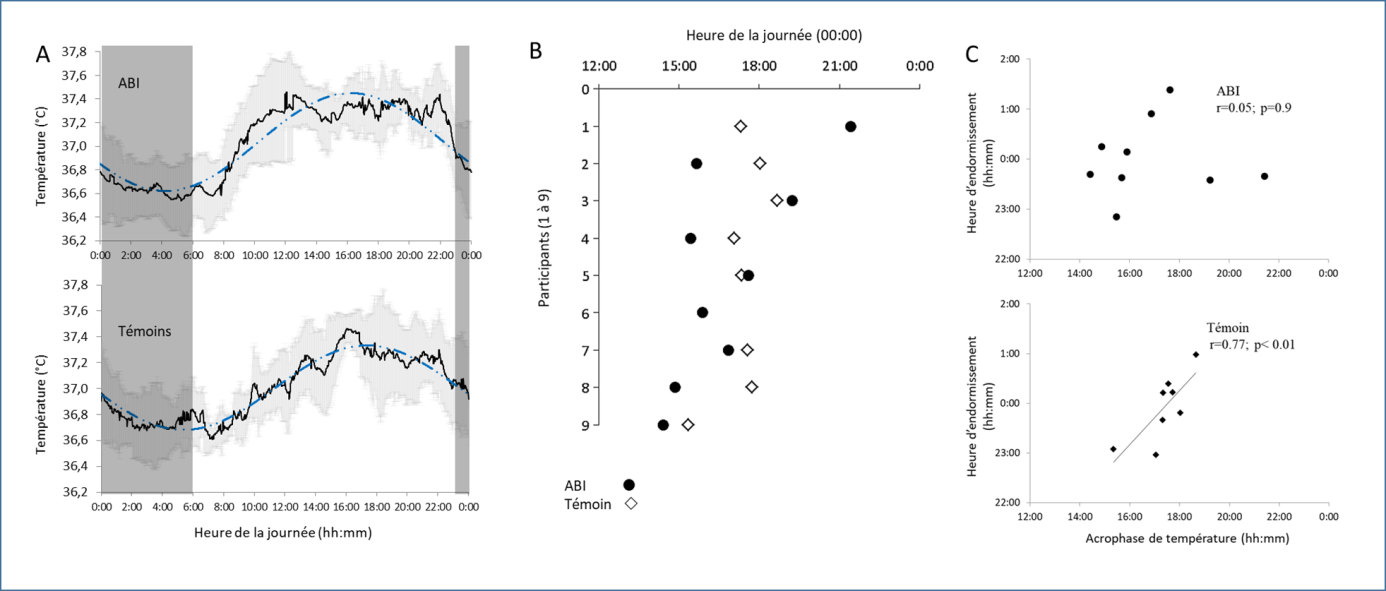
Figure 2 : Résumé des résultats de l’étude de Martin et al., (2016)8, menée avec 9 participants de l’AFVBI. La figure A présente le profil moyen de température enregistré à l’aide d’une capsule intestinale pendant 24h. La courbe noire représente le signal enregistré par la capsule. La courbe bleue représente la modélisation du rythme circadien de température par la méthode d’analyse du « COSINOR ». La zone grise représente la dispersion des données (l’écart-type). Il est intéressant de noter que les participants aréflexiques vestibulaires bilatéraux idiopathique (ABI) ont un rythme de température qui suit moins la modélisation mathématique comparé aux participants témoins. La figure B montre l’acrophase de température de chaque participant ABI et témoin. La dispersion des acrophases est plus importante dans le groupe ABI. Enfin, la figure C montre qu’il n’y a pas de corrélation entre l’acrophase de température et l’heure d’endormissement chez les participants ABI (ce qui atteste d’une désynchronisation entre le rythme de la température et le rythme veille-sommeil) alors que la corrélation entre les deux rythmes était élevée chez les participants témoins.
A partir de ces résultats, nous avons commencé à étudier la possibilité que le système vestibulaire soit lui-même un synchroniseur des rythmes biologiques. Chez l’animal, nous avons montré qu’une stimulation vestibulaire via des expositions hypergravitaires courtes à 2G peut accélérer la resynchronisation du rythme de la température suite à un décalage horaire9. Dans ce domaine chez l’Homme, nous avons démontré qu’une stimulation vestibulaire pouvait modifier les caractéristiques du rythme de l’activité motrice appliquée en fin de journée10.
- Perspectives de recherche
Les résultats novateurs obtenus sur les influences chronobiologiques du système vestibulaire nous incitent à poursuivre nos travaux selon deux axes.
Le premier consiste à préciser les mécanismes d’entrainement de l’horloge. Nos travaux supposent que le système vestibulaire fournit un signal de type actimétrique à l’horloge biologique, expliquant alors pourquoi l’activité physique (qui stimule généralement le système vestibulaire) peut moduler les rythmes circadiens et le sommeil. Cependant, comme nous l’avons évoqué, d’autres facteurs pourraient expliquer l’effet de l’exercice sur l’horloge (température, catécholamine…) et aucune étude n’a pu établir avec certitude l’influence directe du système vestibulaire sur l’horloge biologique. Une étude contrôlée en laboratoire, selon un protocole de mise en évidence de l’activité de l’horloge biologique chez l’Homme reconnu pour étudier les mécanismes de fonctionnement de l’horloge interne (constante routine), au moyen d’un marqueur fidèle (la mélatonine), devient donc nécessaire pour confirmer cette hypothèse. Ces éléments théoriques manquent pour appuyer le développement de programme de réhabilitation des rythmes biologiques et ce projet a donc pour ambition de répondre à cette problématique.
Le second axe, plus appliqué, est de mieux caractériser les troubles chronobiologiques et du sommeil des patients atteints d’une aréflexie vestibulaire bilatérale, d’en comprendre les mécanismes et de proposer des traitements spécifiques.
- Et pour finir, quelques conseils…
Même si les répercussions sur le sommeil et les mécanismes des troubles chronobiologiques que nous avons observés chez les patients souffrant d’une aréflexie vestibulaire bilatérale ne sont pas encore connus, on peut cependant donner quelques conseils pour améliorer la synchronisation des rythmes (renforcer le rôle des synchroniseurs) et la qualité du sommeil des patients :
- Avoir des horaires réguliers : se coucher et surtout se lever à des heures régulières afin de stabiliser l’activité de votre horloge biologique. Pour cela il faut au préalable connaître ses propres besoins de sommeil, ils sont en effet très variables d’une personne à l’autre.
- Profiter au maximum du soleil et de la lumière du jour.
- Pratiquer une activité physique la journée, mais l’arrêter au moins 2 heures avant le coucher. Des résultats récents montrent que pratiquer le matin ou dans la première partie de l’après-midi favorise l’avance de sécrétion de mélatonine, ce qui facilite l’endormissement le soir.
- Eviter si possible l’utilisation d’écran 1 à 2 heures avant votre heure de coucher. En effet, l’exposition à la lumière le soir retarde votre horloge biologique et donc ne favorise pas l’endormissement, c’est le cas en particulier de la lumière bleue des écrans d’ordinateurs et de téléphones mobiles.
- Diminuer les excitants de type caféine et théine après 16 heures.
- Dîner léger (peu gras) AVEC sucres lents et au moins 2 heures avant le coucher.
- Favoriser des activités calmes en fin de journée, instaurer son propre rituel d’endormissement.
- Avoir une bonne literie.
- Optimiser la chambre : aérée, à une température de 18° ou moins, obscure, silencieuse et déconnectée.
- Se coucher dès les 1ers signes de sommeil.
- Limiter le temps passé au lit sans dormir (donc éviter l’utilisation des écrans au lit).
Références
1. Stephan, F. K. & Zucker, I. Circadian rhythms in drinking behavior and locomotor activity of rats are eliminated by hypothalamic lesions. Proc. Natl. Acad. Sci. 69, 1583 (1972).
2. Czeisler, C. A. et al. Stability, precision, and near-24-hour period of the human circadian pacemaker. Science 284, 2177–2181 (1999).
3. Gronfier, C. Le rôle et les effets physiologiques de la lumière : sommeil et horloge biologique dans le travail de nuit et posté. Arch. Mal. Prof. Environ. 70, 253–261 (2009).
4. Bien dormir pour mieux faire face - Enquête INSV/MGEN 2021. INSV Institut National du Sommeil et de la Vigilance https://institut-sommeil-vigilance.org/bien-dormir-pour-mieux-faire-face-enquete-insv-mgen-2021/.
5. Horowitz, S. S., Blanchard, J. H. & Morin, L. P. Intergeniculate leaflet and ventral lateral geniculate nucleus afferent connections: An anatomical substrate for functional input from the vestibulo-visuomotor system. J. Comp. Neurol. 474, 227–245 (2004).
6. Fuller, P. M., Jones, T. A., Jones, S. M. & Fuller, C. A. Neurovestibular modulation of circadian and homeostatic regulation: Vestibulohypothalamic connection? Proc. Natl. Acad. Sci. 99, 15723–15728 (2002).
7. Martin, T. et al. Vestibular loss disrupts daily rhythm in rats. J. Appl. Physiol. Bethesda Md 1985 118, 310–318 (2015).
8. Martin, T. et al. Exploration of Circadian Rhythms in Patients with Bilateral Vestibular Loss. PloS One 11, e0155067 (2016).
9. Martin, T. et al. Vestibular stimulation by 2G hypergravity modifies resynchronization in temperature rhythm in rats. Sci. Rep. 10, (2020).
10. Pasquier, F. et al. Effect of vestibular stimulation using a rotatory chair in human rest/activity rhythm. Chronobiol. Int. 37, 1244–1251 (2020).
Par Christophe Lopez, Chargé de Recherche au CNRS - Laboratoire de Neurosciences Cognitives, CNRS & Aix-Marseille Université
Les signaux vestibulaires, qui informent le cerveau des mouvements et des inclinaisons du corps dans l’espace, sont connus pour leur rôle dans les réflexes oculomoteurs, posturaux et neurovégétatifs. Toutefois, leur contribution ne s’arrête pas là. Les signaux vestibulaires contribuent à de nombreuses facettes de la cognition spatiale, corporelle et émotionnelle (Smith & Zheng 2013; Mast et al. 2014; Lopez 2016). Des travaux récents des neurosciences laissent à penser qu’ils joueraient également un rôle dans les aspects les plus fondamentaux de la conscience de soi (Lenggenhager & Lopez 2015). Ainsi, des patients porteurs d’atteintes du système vestibulaire périphérique ou central peuvent rapporter des modifications de leur perception corporelle, leur sentiment de subjectivité, ou leur personnalité. Des sensations telles que « Mon corps paraît étrange », « Je perds le contrôle de moi-même », « Je ne suis plus dans mon corps » ne sont pas si rares dans les atteintes vestibulaires (Smith & Darlington 2013).
En plus de ces troubles des représentations du soi et du corps, les patients avec des atteintes du système vestibulaire peuvent rapporter des difficultés pour naviguer dans l’espace, c’est-à-dire des difficultés pour coder leurs déplacements, les mémoriser et les restituer. Les processus sensoriels et neuraux de la navigation spatiale sont très complexes car plusieurs sens entrent en jeu en plus du système vestibulaire (la vision, la somesthésie, les signaux issus des commandes motrices) et de nombreuses régions du cerveau sont impliquées. Les chercheurs en neurosciences commencent à mieux comprendre les bases cérébrales de la navigation spatiale, et ces découvertes ont d’ailleurs été couronnées par le Prix Nobel de Physiologie ou Médecine attribué en 2014 à John O’Keefe, May-Britt Moser et Edvard I. Moser.
- Investigations cliniques
Plusieurs études épidémiologiques conduites aux États-Unis indiquent que les troubles des fonctions vestibulaires sont associés à une baisse des performances dans des tâches cognitives dites visuo-spatiales, c’est-à-dire des tâches impliquant de faire des jugements sur des objets ou des scènes présentés sur un écran d’ordinateur ou une feuille de papier (Bigelow et al. 2015). Une étude de référence conduite par l’équipe de Thomas Brandt en Allemagne a montré que des patients avec une perte bilatérale des fonctions vestibulaires présentaient des déficits de mémoire spatiale par rapport à des personnes de même âge et de même sexe avec un système vestibulaire fonctionnant correctement (Brandt et al. 2005). Dans cette étude, la mémoire spatiale a été étudiée par la tâche de la piscine de Morris sur un écran d’ordinateur. On donne aux participants le point de vue qu’ils auraient s’ils se tenaient au centre d’une piscine circulaire remplie d’eau. Autour de la piscine, des repères sont visibles. Il peut s’agir de formes géométriques ou d’une véritable scène d’extérieur. Les participants doivent se déplacer dans cette piscine en utilisant les boutons d’un clavier jusqu’à ce qu’ils trouvent par hasard une plateforme sous la surface de l’eau et non visible. Les participants peuvent repérer la position de cette plateforme par rapport aux références visuelles autour de la piscine. Dans les essais suivants, les participants sont positionnés à un autre endroit de la piscine et on leur demande de retourner à la plateforme qui, elle, n’a pas changé de position. On mesure sur une série d’une dizaine d’essais le temps que les participants mettent pour retrouver la plateforme et la distance parcourue entre leur position de départ et la plateforme. Plusieurs études ont montré qu’une perte vestibulaire bilatérale se traduisait par un retard dans l’apprentissage de la position de la plateforme et par une plus grosse erreur de localisation de la plateforme (Brandt et al. 2005; Kremmyda et al. 2016).
- Modifications cérébrales après atteintes des fonctions vestibulaires
L’une des régions cérébrales les plus étudiées dans le contexte de la navigation spatiale s’appelle l’hippocampe. C’est une structure localisée dans la partie médiale des lobes temporaux. Au début des années 2000, Brandt et ses collaborateurs ont utilisé l’Imagerie par Résonance Magnétique (IRM) pour mesurer le volume de l’hippocampe chez des personnes testées plusieurs années après une perte vestibulaire bilatérale (suite à la section chirurgicale des deux nerfs vestibulaires).
Ils ont ainsi découvert une réduction du volume (une atrophie) de l’hippocampe de 17%, qui était associée aux déficits de mémoire spatiale dans la tâche de la piscine de Morris décrite ci-dessus. L’atrophie de l’hippocampe dans les atteintes vestibulaires a depuis été confirmée par plusieurs études chez des personnes avec une perte vestibulaire bilatérale partielle, un trouble vestibulaire unilatéral aigu ou une maladie de Menière unilatérale (zu Eulenburg et al. 2010; Göttlich et al. 2016; Kremmyda et al. 2016; Seo et al. 2016), mais d’autres études n’ont pas pu confirmer cet effet chez d’autres groupes de patients avec des atteintes vestibulaires (Hüfner et al. 2007; Cutfield et al. 2014).
- Navigation spatiale réelle
Les limites des tâches cognitives décrites précédemment, comme le test de la piscine de Morris en réalité virtuelle, sont qu’elles n’impliquent pas de mouvements du corps entier comme dans la navigation réelle, qu’elles simplifient l’environnement et réduisent les interactions entre le participant et son environnement.
Or les personnes avec des troubles du système vestibulaire sont souvent plus gênées dans leur vie quotidienne lorsqu’il y a beaucoup d’informations à gérer en même temps, et d’autant plus s’il faut se tenir debout ou marcher en même temps. Quelques études récentes ont donc analysé les performances de personnes avec des atteintes bilatérales du système vestibulaire pendant la navigation au sein d’un bâtiment hospitalier contenant plusieurs couloirs, de nombreuses portes, etc. (Schöberl et al. 2021). Les participants portaient un casque permettant d’analyser les mouvements oculaires et de savoir ce qu’ils avaient regardé pendant la navigation. Les résultats de ces études indiquent que les personnes avec une perte vestibulaire bilatérale avaient plus de difficultés pour trouver des raccourcis et pour créer de nouvelles trajectoires de déplacement dans le bâtiment. Toutefois, pour reproduire des trajets appris, ils n’avaient pas plus de difficulté que des participants contrôles. L’étude a également révélé que le comportement et les stratégies de navigation différaient chez les patients avec perte vestibulaire bilatérale et chez les contrôles. En effet, les patients passaient moins de temps aux intersections entre les couloirs et les patients avaient tendance à fixer moins d’objets.
- Conclusions et perspectives
Les troubles de la navigation spatiale, bien qu’ils ne constituent pas la doléance principale des patients avec une atteinte vestibulaire, sont une réalité mesurable. Toutefois, leur prévalence n’est pas connue.
Il reste également à comprendre les facteurs qui font que certaines personnes avec un trouble vestibulaire présentent des déficits objectifs et/ou des plaintes concernant la navigation spatiale et pourquoi d’autres n’en présentent pas.
Références
Bigelow RT, Semenov YR, Trevino C, Ferrucci L, Resnick SM, Simonsick EM, Xue Q-L, Agrawal Y. 2015. Association between visuospatial ability and vestibular function in the Baltimore longitudinal study of aging. J Am Geriatr Soc. 63:1837–1844.
Brandt T, Schautzer F, Hamilton DA, Bruning R, Markowitsch HJ, Kalla R, Darlington C, Smith P, Strupp M. 2005. Vestibular loss causes hippocampal atrophy and impaired spatial memory in humans. Brain. 128:2732–2741.
Cutfield NJ, Scott G, Waldman AD, Sharp DJ, Bronstein AM. 2014. Visual and proprioceptive interaction in patients with bilateral vestibular loss. Neuroimage Clin. 4:274–282.
Göttlich M, Jandl NM, Sprenger A, Wojak JF, Münte TF, Krämer UM, Helmchen C. 2016. Hippocampal gray matter volume in bilateral vestibular failure. Hum Brain Mapp. 37:1998–2006.
Hüfner K, Hamilton DA, Kalla R, Stephan T, Glasauer S, Ma J, Bruning R, Markowitsch HJ, Labudda K, Schichor C, Strupp M, Brandt T. 2007. Spatial memory and hippocampal volume in humans with unilateral vestibular deafferentation. Hippocampus. 17:471–485.
Kremmyda O, Hüfner K, Flanagin VL, Hamilton DA, Linn J, Strupp M, Jahn K, Brandt T. 2016. Beyond Dizziness: Virtual Navigation, Spatial Anxiety and Hippocampal Volume in Bilateral Vestibulopathy. Front Hum Neurosci. 10:139.
Lenggenhager B, Lopez C. 2015. Vestibular contributions to the sense of body, self, and others. In: Metzinger T,, Windt JM, editors. Open MIND. Frankfurt am Main: MIND-Group. p. 1–38.
Lopez C. 2016. The vestibular system: balancing more than just the body. Curr Opin Neurol. 29:74–83.
Mast FW, Preuss N, Hartmann M, Grabherr L. 2014. Spatial cognition, body representation and affective processes: the role of vestibular information beyond ocular reflexes and control of posture. Front Integr Neurosci. 8:44.
Schöberl F, Pradhan C, Grosch M, Brendel M, Jostes F, Obermaier K, Sowa C, Jahn K, Bartenstein P, Brandt T, Dieterich M, Zwergal A. 2021. Bilateral vestibulopathy causes selective deficits in recombining novel routes in real space. Sci Rep. 11:2695.
Seo YJ, Kim J, Kim SH. 2016. The change of hippocampal volume and its relevance with inner ear function in Meniere’s disease patients. Auris Nasus Larynx. 43:620–625.
Smith PF, Darlington CL. 2013. Personality changes in patients with vestibular dysfunction. Front Hum Neurosci. 7:678.
Smith PF, Zheng Y. 2013. From ear to uncertainty: vestibular contributions to cognitive function. Front Integr Neurosci. 7:84.
zu Eulenburg P, Stoeter P, Dieterich M. 2010. Voxel-based morphometry depicts central compensation after vestibular neuritis. Ann Neurol. 68:241–249.
Jean-Philippe Guyot
- Une fonction vestibulaire artificielle pour bientôt ?
- La piste biologique : régénérescence des cellules sensorielles Dans la toute grande majorité des cas, la perte de la fonction vestibulaire résulte de la dégénérescence des cellules sensorielles de l’oreille interne, cellules qui transforment les accélérations en signaux électriques transmis au cerveau par le nerf vestibulaire. C’est pourquoi, des équipes travaillent à faire ‘renaître’ les cellules sensorielles de l’appareil vestibulaire. Certaines ont réussi à les régénérer chez des rongeurs [1], d’autres sur des tissus de l’appareil vestibulaire humain, en éprouvettes [2].
- La piste des neuroprothèses
Neuroprothèses substitutives
Ces dernières décennies, des équipes ont développé des ceintures portées à la taille, munies de capteurs de position déclenchant une alarme acoustique [3] ou vibratoire [4, 5] d’autant plus intense que la posture du sujet s’éloigne de la verticale. Malheureusement, les informations que donnent ces prothèses ne peuvent pas se substituer à celles du système vestibulaire, très rapide, puisqu’elles transitent par les voies neurologiques de modalités sensorielles lentes, l’audition et la sensibilité. Dès lors, elles ne peuvent pas donner de résultats très satisfaisants.Neuroprothèses vestibulaires
Depuis le milieu des années 80, il est possible de redonner une audition aux sourds profonds par un ‘implant cochléaire’. Cette prothèse est faite d’un microphone, d’un processus électronique transformant les sons en signaux électriques, en remplacement de la cochlée, et d’électrodes implantées chirurgicalement au contact du nerf auditif.
Début 2000, il a paru logique à un physiologiste de l’université Harvard à Boston (USA), Daniel Merfeld, de développer, sur un concept comparable, un implant vestibulaire pour restituer la fonction d’équilibre aux patients souffrant d’une perte bilatérale de la fonction vestibulaire [6]. Vu les résultats prometteurs qu’il a très vite obtenus chez l’animal, il a invité l’équipe de médecins de Genève, intéressée par le projet et maitrisant les approches chirurgicales de l’oreille interne nécessaires à sa réalisation, à se joindre à son groupe. Ainsi, après un séjour de quelques semaines à Boston pour mettre au point le plan de recherche, les premiers essais chez l’homme ont débuté à Genève où des membres de l’équipe de Daniel Merfeld venaient, au besoin.
En 2010, Genève a invité l’équipe de Herman Kingma de Maastricht à se joindre à elle pour renforcer le groupe. La collaboration entre les deux institutions continue et le groupe est connu sous l’appellation « Geneva-Maastricht Group ». Depuis 2005, une deuxième équipe travaille au même développement, celle de Charley Della Santina de l’université Johns Hopkins à Baltimore (USA) [7]. Où en est-on ? En 2014, l’équipe Genève-Maastricht montrait que le réflexe vestibulo-oculaire était rétabli par la neuroprothèse [8] et que les patients recouvraient une vision normale à la marche [9], résultats confirmés en 2019 par la première publication d’une implantation chez l’homme de l’équipe de Baltimore [10]. Depuis, il a été prouvé que les réflexes nécessaires au maintien de la posture sont aussi restitués [11]. Toutefois, plusieurs étapes doivent encore être franchies avant la mise en application clinique d’un implant vestibulaire telle que contrôler les interactions électriques entre les électrodes [12], évaluer le risque de perte d’audition consécutif à l’insertion d’électrodes à proximité de la cochlée (par prudence, jusqu’ici, le prototype d’implant vestibulaire n’a été testé que dans des oreilles sourdes), etc.. Heureusement, la firme Med El (manufacture d’implant cochléaire à Innsbruck, Autriche) est aujourd’hui très impliquée dans le développement de la neuroprothèse et concourt aux avancées aussi bien de l’équipe européenne que celles de l’équipe américaine. Alors, une application clinique, pour quand ?Remerciements
Le groupe Genève-Maastricht a été ou est financé en partie par la Communauté européenne (7e programme-cadre, thème 3, Technologies de l'information et de la communication), le Fonds national suisse de la science Sinergia et la firme Med El, Innsbruck, Autriche.
Références
1. Burns JC, Stone JS. Development and regeneration of vestibular hair cells in mammals. Semin Cell Dev Biol 2017;65:96-105.
2. Taylo RR, Filia A, Paredes U, AsaiY, Holt JR, Lovett M, Forge A. Regenerating hair cells in vestibular sensory epithelia from humans. Elife 2018;18; 7:e34817.
3. Hegeman J, Honegger F, Kupper M, Allum JH. The balance control of bilateral peripheral vestibular loss subjects and its improvement with auditory prosthetic feedback. J Vestib Res. 2005;15:109–117.
4. Wall C, 3rd, Weinberg MS, Schmidt PB, Krebs DE. Balance prosthesis based on micromechanical sensors using vibrotactile feedback of tilt. IEEE Trans Biomed Eng. 2001;48:1153–1161.
5. Janssen M, Pas R, Aarts J, Janssen-Potten Y, Vles H, Nabuurs C, van Lummel R, Stokroos R, Kingma H. Clinical observational gait analysis to evaluate improvement of balance during gait with vibrotactile biofeedback. Physiother Res Int 2012;17:4–11.
6. Gong W, Merfeld DM. Prototype neural semicircular canal prosthesis using patterned electrical stimulation. Ann Biomed Eng. 2000;28:572–581.
7. Della Santina C, Migliaccio A, Patel A. Electrical stimulation to restore vestibular function development of a 3-d vestibular prosthesis. Conf Proc IEEE Eng Med Biol Soc 2005; 2005:7380-5.
8. Perez Fornos A, Guinand N, Van De Berg R, Stokroos RJ, Micera S, Kingma H, Pelizzone M, Guyot JPh. Artificial balance: restoration of the vestibulo-ocular reflex in humans with a prototype vestibular neuroprosthesis. Front Neuro Otol 2014;10:33–89.
10. Guinand N, Van de Berg R, Cavuscens S, Stokroos R, Ranieri M, Pelizzone M, KingmaH, Guyot JPh, Pérez Fornos A. Restoring visual acuity in dynamic conditions with a vestibular implant. Front Neurosci 2016 ; 22;10:577.
11. Boutros PJ, Schoo DP, Rahman M, Valentin NS, Chow MR, Ayiotis AI, Morris BJ, Hofner A, Rascon AM, Marx A, Deas R, Fridman GY, Davidovics NS, Ward BK, Treviño C, Bowditch SP, Roberts DC, Lane KE, Gimmon Y, Schubert MC, Carey JP, Jaeger A, Della Santina CC. Continuous vestibular implant stimulation partially restores eye-stabilizing reflexes. JCI Insight 2019 Nov 14;4(22):e128397.
12. Perez Fornos A, van de Berg R, Armand S, Cavuscens S,Ranieri M, Crétallaz C, Kingma H, Guyot JPh, Guinand N. Cervical myogenic potentials and controlled postural responses elicited by a prototype vestibular implant. J Neurol 2019; 266(Suppl 1):33-41.
13. Boutabla A, Cavuscens S, Ranieri M, Crétallaz C, Kingma H, Van de Berg R, Guinand N, Pérez Fornos A. Simultaneous activation of multiple vestibular pathways upon electrical stimulation of semicircular canal afferents. J Neurol 2020; 267(Suppl 1):273-284.
- VBI et perception sonore (influence des sons forts ?)
- VBI et vision (verres progressifs ou non ?)
- VBI et troubles du sommeil
- VBI et hippocampe (une « rééducation » hippocampique ?)
- VBI et retentissement psychologique : baisse de l’estime de soi, honte, anxiété/futur, dépression…
- VBI serait-elle la conséquence d’un traumatisme psychologique ?
- VBI et émotivité (approche intégrative)
- VBI et mémoire procédurale
- VBI et mémoire perceptive
- VBI et vieillissement : étude longitudinale
- VBI et date d’apparition : congénitale ou acquise ? Chez l’enfant ou chez l’adulte ?
- VBI : la symptomatologie varie-t-elle en fonction de la localisation de l’atteinte (canaux semi-circulaires, utricule, saccule ?). Pourquoi une atteinte labyrinthique isolée (le plus souvent limitée au Pars Superior) sans atteinte cochléaire ?
- VBI et perte d'équilibre (plus de chutes ? Dans quelles situations ? Gravité ?...)
- VBI et parcours COVID
- Les ressources humaines pour les malades et les professionnels de santé
Association Française de Vestibulopathie Bilatérale idiopathique : AFVBI
https://www.afvbi.info
- Cette association a pour but de :
- rompre l'isolement, constituer un réseau de soutien et d'entraide entre les adhérents ;
- évaluer l'impact de l'affection sur les plans psychologique, familial, socioprofessionnel et le coût en termes de santé publique ;
- contribuer à améliorer la connaissance de la maladie auprès des pouvoirs publics, des professionnels de santé et du grand public ;
- faire reconnaître la vestibulopathie bilatérale idiopathique comme handicap sensoriel ; faciliter les travaux de recherche.
Association Suisse du Déficit Vestibulaire Bilatéral
https://asdvb.ch
Société Internationale de Rééducation Vestibulaire : SIRV
Société Française de Kinésithérapie Vestibulaire : SFKV
- Le Groupement de Recherche Physiopathologie Vestibulaire ou GDR Vertige
- Alliance maladies rares
https://www.alliance-maladies-rares.org
La liste ci-dessous n’est pas exhaustive. Elle est constituée des professionnels avec qui l’AFVBI travaille de façon régulière.
Le malade peut consulter son ORL local. De plus, en 2022, un centre de référence (CRMR) à Paris sous la direction du Dr Charlotte HAUTEFORT et un réseau de centres de compétence soins maladies rares (CCMR) dédiés aux vestibulopathies sont en voie de constitution.
- Publications
Interference between walking and a cognitive task is increased in patients with bilateral vestibular loss.
Gait Posture. 2012 Jun;36(2):319-21.
Action representation in patients with bilateral vestibular impairments.
PLoS One. 2011;6 (10):e26764.
Vestibular atelectasis: Myth or reality?
Laryngoscope. 2019 Jul;129(7):1689-1695. doi: 10.1002/lary.27793. Epub 2019 Jan 10. PMID: 30632154
MRI Evidence of Vestibular Atelectasis in Bilateral Vestibulopathy and Tullio Phenomenon.
Otol Neurotol. 2019 Oct;40(9):e944-e946. doi: 10.1097/MAO.0000000000002409. PMID: 31469790
Electrophysiological and inner ear MRI findings in patients with bilateral vestibulopathy
European Archives of Oto-Rhino-Laryngology https://doi.org/10.1007/s00405-020-05829-8 OTOLOGY
Recent advances in idiopathic bilateral vestibulopathy : a literature review.
Orphanet J Rare Diseases 2019; Vol 14 (202)
Effect of Rotating Auditory Scene on Postural Control in Normal Subjects, Patients with Bilateral Vestibulopathy, Unilateral, or Bilateral Cochlear Implants.
Front Neurol. 2018 Nov 16;9: 972. doi: 10.3389/fneur.2018.00972. eCollection 2018. PMID: 30505289 Free PMC article.
Vergence and Standing Balance in Subjects with Idiopathic Bilateral Loss of Vestibular Function.
PLoS One. 2013 Jun 18;8(6): e66652.
Vestibulo-sympathetic reflex in patients with bilateral vestibular loss.
J Appl Physiol (1985). 2019 Sep 12. doi: 10.1152/japplphysiol.00466.2019. Online ahead of print. PMID: 31513442
Vestibular compensation: the neuro-otologist's best friend.
J Neurol. 2016 Apr;263 Suppl 1:S54-64. doi: 10.1007/s00415-015-7903-4. Epub 2016 Apr 15. PMID: 27083885
Rehabilitation of dynamic visual acuity in patients with unilateral vestibular hypofunction: earlier is better.
Eur Arch Otorhinolaryngol. 2020 Jan;277(1):103-113. doi: 10.1007/s00405-019-05690-4. Epub 2019 Oct 21. PMID: 31637477
How Eye Movements Stabilize Posture in Patients With Bilateral Vestibular Hypofunction.
Front Neurol. 2018 Sep 18;9:744. doi: 10.3389/fneur.2018.00744. eCollection 2018. PMID: 30279673 Free PMC article.
Interaction between Vestibular Compensation Mechanisms and Vestibular Rehabilitation Therapy: 10 Recommendations for Optimal Functional Recovery.
Front Neurol. 2015 Jan 6;5:285. doi: 10.3389/fneur.2014.00285. eCollection 2014. PMID: 25610424
Bilateral vestibulopathy: Diagnostic criteria Consensus document of the Classification Committee of the Bárány Society.
J Vestib Res. 2017;27(4):177-189. doi: 10.3233/VES-170619.
Is vestibular neuritis a human model of compensation,
Clinical perspectives and vestibular rehabilitation
Dans vestibular compensation: facts, theories and clinical perspectives
Toupet M, Van Nechel C, Bozorg Grayeli A.
Influence of body laterality on recovery from Subjective Visual Vertical tilt after vestibular neuritis
Audiol Neurootol. 2014;19(4):248-55.
Vestibular rehabilitation in the elderly
In « Rehabilitative management of the dizzy patient » G.Guidetti editor,
Experta Medica, Milano, Italy, 2000, (pp 143-166)
Subjective Visual Vertical in Idiopathic Bilateral Vestibular Hypofunction: Enhanced Role of Vision, Neck, and Body Proprioception.
Otol Neurotol. 2017 Aug;38(7):1010-1016. doi: 10.1097/MAO.0000000000001462. PMID: 28598949
The Subjective Visual Vertical
Advance in Oto-Rhino-Laryngology, Karger, Basel 2001, 58: 77-87
Visual Input Is the Main Trigger and Parametric Determinant for Catch-Up Saccades During Video Head Impulse Test in Bilateral Vestibular Loss.
Front Neurol. 2019 Jan 4;9: 1138. doi: 10.3389/fneur.2018.01138. eCollection 2018. PMID: 30662427 Free PMC article.
Role of Inner Ear in Self and Environment Perception.
Front Neurol. 2020 Feb 20;11:22. doi: 10.3389/fneur.2020.00022. eCollection 2020. PMID: 32153485 Free PMC article.
|